תוֹכֶן
- TL; DR (יותר מדי זמן; לא קרא)
- סיווג פרופאן
- נוסחה כימית של פרופאן
- מבנה פרופאן
- מאפייני פרופאן
- שימושים בפרופן
פרופאן הוא דלק מאובן ורכיב בגז טבעי. במשך מיליוני שנים הוא נוצר משרידים אורגניים של אורגניזמים ונכרות מפיקדונות תת קרקעיים. גז הפרופן הוא תרכובת אורגנית העשויה משלוש מולקולות של אטומי פחמן המלווים בשמונה אטומי מימן. סוג קשרי הפחמן-פחמן-מימן קובע את המבנה של מולקולות פרופאן, העוקב אחר אותה תבנית כמו סוגים אחרים של גזים טבעיים כמו מתאן ובוטאן.
TL; DR (יותר מדי זמן; לא קרא)
TL; DR (יותר מדי זמן; לא קרא)
הנוסחה הכימית של פרופאן היא C3ח8.
סיווג פרופאן
פרופאן מסווג כתרכובת אורגנית מכיוון שהוא מכיל פחמן. זה מסווג עוד יותר כפחמימן מכיוון שהוא שייך לקבוצה של תרכובות אורגניות העשויות רק מפחמן ומימן. ליתר דיוק, פרופאן הוא סוג של פחמימנים הנקרא אלקן. האטומים במולקולות אלקן מוחזקים יחד על ידי קשרים קוולנטיים יחידים, ואטומי הפחמן מהווים תמיד ארבעה קשרים קוולנטיים.
נוסחה כימית של פרופאן
אלקנים עוקבים אחר נוסחה כללית עם יחס קבוע של אטומי פחמן לאטומי מימן: C_nח2_n+2. האלקן הפשוט ביותר הוא מתאן, המכונה גם גז טבעי. הוא מכיל אטום פחמן אחד הקשור לארבעה אטומי מימן. עבור מתאן, n = 1, כך שמספר אטומי המימן שיש לו שווה ל 2 (1) +2 השווה ל 4. אתאן מכיל שני אטומי פחמן הקשורים זה לזה, וכל פחמן נקשר לשלושה אטומי מימן בסך הכל שישה אטומי מימן. לפרופן יש שרשרת של שלושה אטומי פחמן, עם נוסחה כימית של C3ח8מכיוון שרשת של שלוש פחמימות דורשת 2 (3) + 2 אטומי מימן, השווים לשמונה. לבוטאן, אלקן נפוץ נוסף המשמש כדלק בפידים גז ידניים, יש ארבעה אטומי פחמן הקשורים לעשרה אטומי מימן, עם נוסחה כימית של C4ח10.
מבנה פרופאן
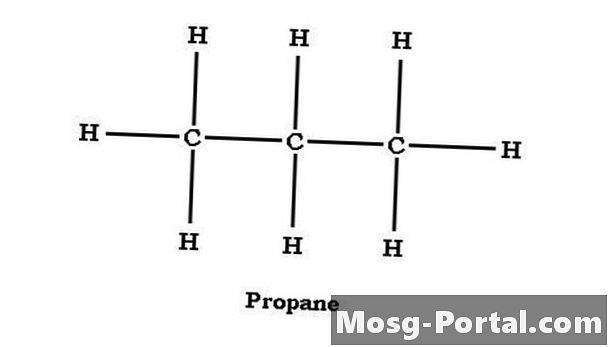
אלקנות יכולות להיות מובנות כרשת ישר או מסועפת. פרופאן הוא אלקן בעל שרשרת ישר, עם אטומי הפחמן מובנים C-C-C. הפחמן האמצעי חולק קשר אחד עם כל אחד מפחמן הקצה ויש לו שני אטומי מימן. פחמימות הקצה כל אחת חולקת קשר עם אטום הפחמן המרכזי ונקשרת כל אחת לשלושה אטומי מימן. מבחינת אטומי פחמן בודדים, פרופאן יכול לבוא לידי ביטוי כ- CH3CH2CH3, המקבילה ל- C3ח8 אך הופך את מבנה הפרופנים למפורש יותר.
מאפייני פרופאן
בנוסף לדמיון המבני המשותף לאלקנים בעלי שרשרת ישר, הם גם חולקים תכונות דומות. פרופאן ופחמימנים אחרים אינם קוטביים. מאפיין זה מכתיב שהם יכולים לערבב רק עם חומרים אחרים שאינם קוטביים. לדוגמא, שמנים ודלקים אחרים עשויים מתערובת של פחמימנים. הם לא יתערבבו עם חומר קוטבי כמו מים; המשיכה בין המולקולות מפרידה בין מים למים. עם אלקנים בעלי שרשרת ישר, נקודת הרתיחה ונקודת ההיתוך גדלות ככל שמספר מולקולות הפחמן גדל. נקודת הרתיחה של הפרופן היא -44 מעלות פרנהייט (-42 מעלות צלזיוס) והתכה של −306 מעלות פרנהייט (−189 מעלות צלזיוס). למתאן, עם פחמן אחד בלבד, יש נקודת רתיחה נמוכה יותר מאשר פרופאן בגודל 164 מעלות צלזיוס. לאוקטן שמונה פחמימות ונקודת רתיחה של 98 מעלות צלזיוס.
שימושים בפרופן
בגלל נקודת הרתיחה הנמוכה, פרופאן נמצא בדרך כלל במצבו הגזי. כאשר מוחלים את הכמות הנכונה של הלחץ והטמפרטורה על פרופאן, הוא עובר תהליך שנקרא נזילה שמכריח גז פרופאן למצב הנוזל שלו. ניתן לאחסן פרופאן כנוזל במיכלים בלחץ, הרבה מעל נקודת הרתיחה שלו. גז פרופאן מנוזל משמש כדלק חימום שנשרף לתנורים חשמליים ומחממי מים חמים. הוא משמש גם כדלק לבישול על גריל גז חיצוני ותנורי בישול קמפינג המונעים על ידי גז. גז פרופאן הוא גם מרכיב במונעים המשמשים בפחי תרסיס. פרופאן משמש גם כמרכיב בסוגים מסוימים של דבקים, חומרי איטום וצבע.